生物催化係列 — 醛縮酶
- 分類:行業動態
- 發布時間:2025-08-22 13:21
- 訪問量:
【概要描述】醛縮酶(aldolase)是裂解酶的一種,可以有效地催化供體(ti) 酮或醛對受體(ti) 醛的立體(ti) 選擇性加成。
生物催化係列 — 醛縮酶
【概要描述】醛縮酶(aldolase)是裂解酶的一種,可以有效地催化供體(ti) 酮或醛對受體(ti) 醛的立體(ti) 選擇性加成。
- 分類:行業動態
- 發布時間:2025-08-22 13:21
- 訪問量:
醛縮酶介紹:
醛縮酶(aldolase)是裂解酶的一種,可以有效地催化供體(ti) 酮或醛對受體(ti) 醛的立體(ti) 選擇性加成。
根據醛縮酶對供體(ti) 的專(zhuan) 一性不同,可分為(wei) 乙醛依賴型醛縮酶、磷酸二羥丙酮(DHAP)依賴型醛縮酶、二羥基丙酮(DHA)依賴型醛縮酶、丙酮酸/磷酸稀醇式丙酮酸依賴型醛縮酶和甘氨酸依賴型醛縮酶等五類醛縮酶。根據酶的催化機理,醛縮酶又可以分為(wei) I 類醛縮酶和II 類醛縮酶[1]:I 類醛縮酶活性中心的賴氨酸會(hui) 與(yu) 羰基共價(jia) 連接形成席夫堿,隨後進攻受體(ti) 醛;II 類醛縮酶活性中心的組氨酸會(hui) 與(yu) 金屬離子(通常為(wei) Zn2+)結合,形成路易斯酸後,結合底物上的醛基發生催化反應[2,3]。
DERA醛縮酶是2-脫氧核糖-5-磷酸醛縮酶 (2-deoxyribose-5-phosphate aldolase, DERA),屬於(yu) 乙醛依賴型醛縮酶。DERA與(yu) 其它醛縮酶的區別在於(yu) 它催化的底物都是醛類,可以催化連續的醛縮反應,如圖1。DERA屬於(yu) I類醛縮酶,常存在於(yu) 高等生物中,一般是分子量為(wei) 160 kDa 的四聚體(ti) ,每個(ge) 亞(ya) 基均為(wei) (α/β)8桶狀結構[4]。這類酶中參與(yu) 形成席夫堿的關(guan) 鍵活性氨基酸殘基為(wei) Asp102,Lys167和Lys201[5]。
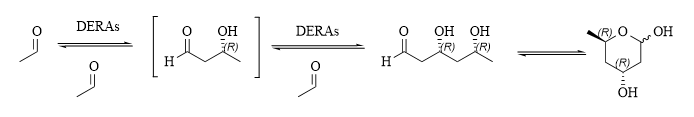
圖1. DERA催化連續醛縮反應
該酶已被應用於(yu) 合成不同藥物中間體(ti) ,包括降膽固醇藥物、抗癌藥物等中間體(ti) 。

實例2、製備阿托伐他汀(降膽固醇藥物)的雙手性中間體(ti) [7]
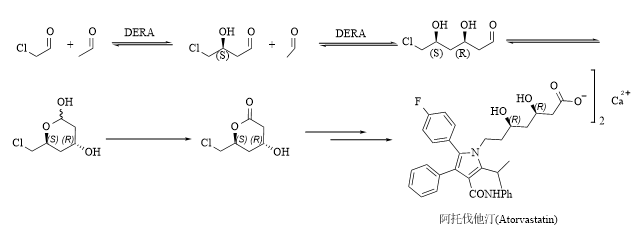
實例3、合成埃博黴素A(抗癌藥物)中間體(ti) [8]
①合成埃博黴素A中間體(ti) 1
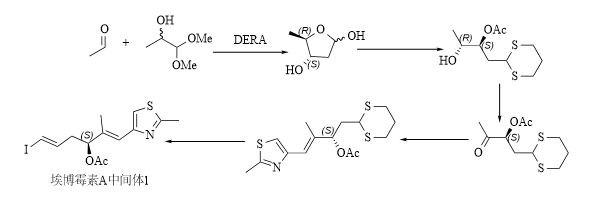
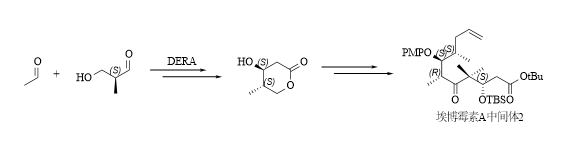
醛縮酶作為(wei) 綠色生物催化劑,可以在溫和條件下合成出新的C-C鍵,且具有立體(ti) 選擇性。同昂貴的金屬催化劑相比,醛縮酶催化具有更經濟、更環保的優(you) 勢。
醛縮酶的催化機理[9]:
DERA醛縮酶活性中心Lys167上的ε-氨基和供體(ti) 上的羰基結合,形成烯胺中間體(ti) ,然後攻擊受體(ti) 羰基碳的Re麵,形成新的C-C鍵,並產(chan) 生R構型的立體(ti) 中心。活性位點附近的水分子和兩(liang) 個(ge) 氨基酸殘基(Asp102,Lys201)組成了質子延遲係統,不僅(jin) 為(wei) 供體(ti) 乙醛C2位上的亞(ya) 胺和烯胺的質子重排提供質子,還為(wei) 後續C3位上的羥基質子化提供質子,詳見圖2。
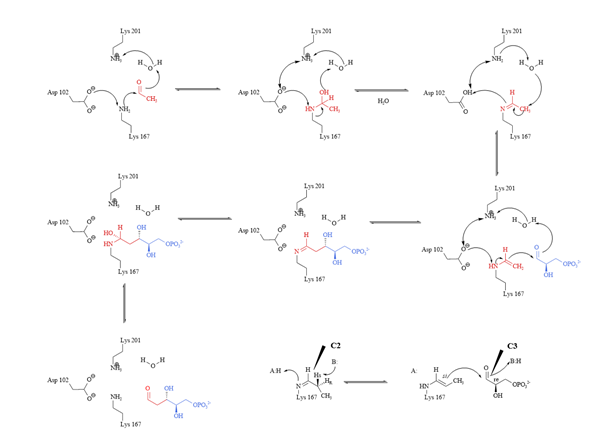
圖2. DERA的催化機理
醛縮酶酶庫和酶開發服務:
304am永利集团生物從(cong) 2007年來就專(zhuan) 注於(yu) 生物酶和生物催化技術以及合成生物學技術的開發與(yu) 應用研究。304am永利集团生物現有的醛縮酶酶庫(304am永利集团生物代號:ES-DERA)中包含12種不同的醛縮酶,可以為(wei) 客戶提供酶篩選、酶促反應工藝優(you) 化、酶改造和生產(chan) 供應等服務。
參考文獻:
[1]李子傑, 利用磷酸二羥基丙酮依賴型醛縮酶在體(ti) 外和體(ti) 內(nei) 進行稀有單糖的合成. [D]. 山東(dong) : 山東(dong) 大學, 2012.
[2]Cowan D A. Comp Biochem Physiol A Physiol, 1997, 118(3) : 429-438.
[3]Hao J, Berry A. Protein Eng Des Sel, 2004, 17(9) : 689-697.
[4]闞葉依, 醛縮酶催化含氟模塊的碳鏈延長. [D]. 四川: 四川大學, 2021.
[5]Heine, A., G. DeSantis, J. G. LuZ, M. et al. Science, 294: 369-374.
[6]Gijsen H J M, Wong C H. Journal of the American Chemical Society. 1994, 116(18): 8422-8423.
[7]Jenneweinl S, Schtirmann M, et al. Biotechnology Advances, 2006, 1: 537-548.
[8]Junjie L and Chi-Huey W. Angew. Chem. 2002, 114: 1462-1465.
[9]陳琦, 羧酸酶的分子改造和突變酶的酶學性質研究. [D]. 浙江: 浙江大學, 2019.
搜索


-
-

