生物催化係列酶介紹之一腈水合酶
- 分類:行業動態
- 發布時間:2025-02-28 09:17
- 訪問量:
【概要描述】腈水合酶(Nitrile hydratase, NHase)是一類作用於(yu) 腈類化合物碳氮三鍵,生成相應的酰胺類化合物的金屬酶。
生物催化係列酶介紹之一腈水合酶
【概要描述】腈水合酶(Nitrile hydratase, NHase)是一類作用於(yu) 腈類化合物碳氮三鍵,生成相應的酰胺類化合物的金屬酶。
- 分類:行業動態
- 發布時間:2025-02-28 09:17
- 訪問量:
一、腈水合酶酶簡介
腈水合酶(Nitrile hydratase, NHase)是一類作用於(yu) 腈類化合物碳氮三鍵,生成相應的酰胺類化合物的金屬酶。
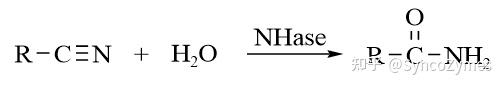
腈水合酶一般由α和β兩(liang) 個(ge) 亞(ya) 基組成,其基因簇下遊通常還存在一個(ge) 幫助其攝取金屬離子的激活蛋白,以促進腈水合酶的成熟。根據酶活性中心結合金屬離子的差異,腈水合酶分為(wei) 鈷型腈水合酶(Co-NHases)和鐵型腈水合酶(Fe-NHases),分別結合了三價(jia) 低自旋的非咕啉鈷和三價(jia) 低自旋的非卟啉鐵[1-4]。
不論是Co-NHase還是Fe-NHase,腈水合酶都含有高度保守的氨基酸序列(Cys-X-X-Cys-Ser-Cys),能夠形成“爪狀”結構,並與(yu) 金屬離子特異性結合,構成活性中心。而Co-NHase與(yu) Fe-NHase的不同點在於(yu) Co-NHase爪狀結構正上方為(wei) 水分子,而Fe-NHase則為(wei) 一氧化氮分子[5]。
實例1、合成酰胺 [6]
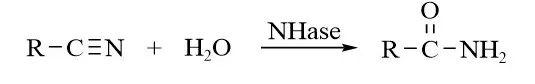
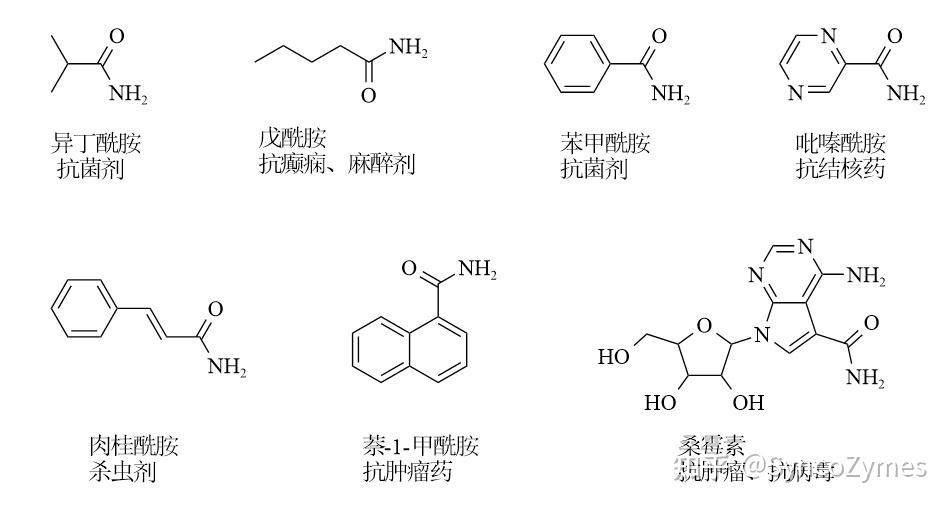
酰胺類產(chan) 品在工業(ye) 、農(nong) 業(ye) 及醫藥等領域有著極大的應用價(jia) 值。丙烯酰胺和煙酰胺等小體(ti) 積酰胺化合物可作為(wei) 大宗化學品,而大體(ti) 積酰胺類化合物通常是高價(jia) 值藥品的原料和醫藥中間體(ti) (見圖1)。
實例2、與(yu) 酰胺酶偶聯生成異羥肟酸[7]
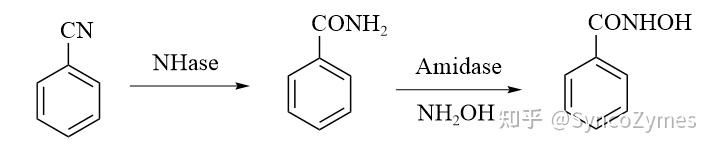
在醫藥領域,異羥肟酸化合物可用於(yu) 治療癌症、關(guan) 節炎、哮喘、機體(ti) 潰爛等疾病[8]。
NHase作為(wei) 綠色生物催化劑,在合成酰胺類化合物方麵具有諸多優(you) 勢:①反應沒有副產(chan) 物形成;②反應為(wei) 一步酶法,工藝簡單;③反應條件溫和。
二、腈水合酶催化機理[9]
目前,認可度較高的腈水合酶催化機理有四種(機理1-4),除了機理4是基於(yu) P. thermophila JCM 3095 腈水合酶與(yu) 底物的複合晶體(ti) 結構數據進行推測的,其餘(yu) 機理均是直接介於(yu) 水分子參與(yu) 的推測。
機理1、內(nei) 球機製
底物氰基上的氮原子與(yu) 酶活性中心的金屬離子形成配位鍵,水分子作為(wei) 親(qin) 核試劑直接進攻底物氰基上的碳原子,形成酰胺鍵(見圖2)。
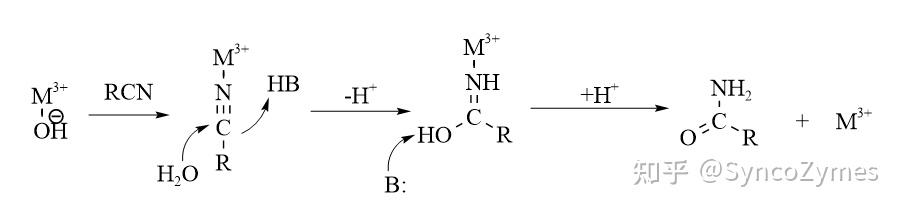
機理2、外球機製
水分子在腈水合酶的活性中心被極化,解離出氫氧根離子。該氫氧根離子與(yu) 金屬離子配位後,攻擊底物氰基上的碳原子,生成了過渡態產(chan) 物(R-C(-OH)=NH)。最後,過渡態產(chan) 物重排後得到酰胺產(chan) 物(見圖3)。
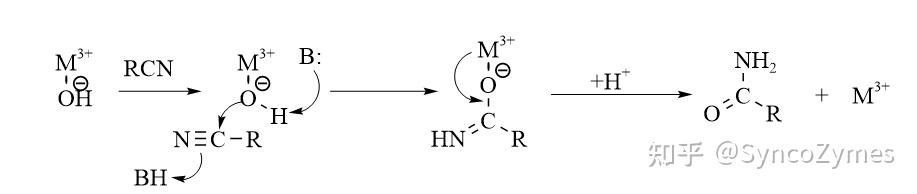
機理3、次外層機製
和外球機製不同,氫氧根離子與(yu) 金屬離子配位後,會(hui) 先活化附近的水分子,再通過該水分子的羥基親(qin) 核攻擊底物。在該過程中,金屬離子的配位層不發生變化(見圖4)。
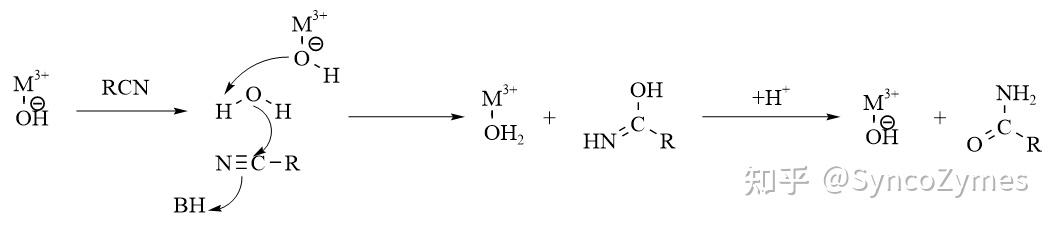
機理4、基於(yu) 腈水合酶與(yu) 底物複合晶體(ti) 結構建立的機製
腈水合酶中的第113位半胱氨酸殘基被氧化為(wei) 半胱氨酸-次磺酸後,會(hui) 親(qin) 核攻擊與(yu) 金屬離子配位的底物,形成過渡態產(chan) 物(R-C(-OH)=NH)中間體(ti) 。該中間體(ti) 一旦發生質子轉移,過渡態產(chan) 物上的碳原子(pathway A)或αCys113(pathway B)在受到水分子的親(qin) 核攻擊時,最終異構化為(wei) 酰胺(見圖5)。
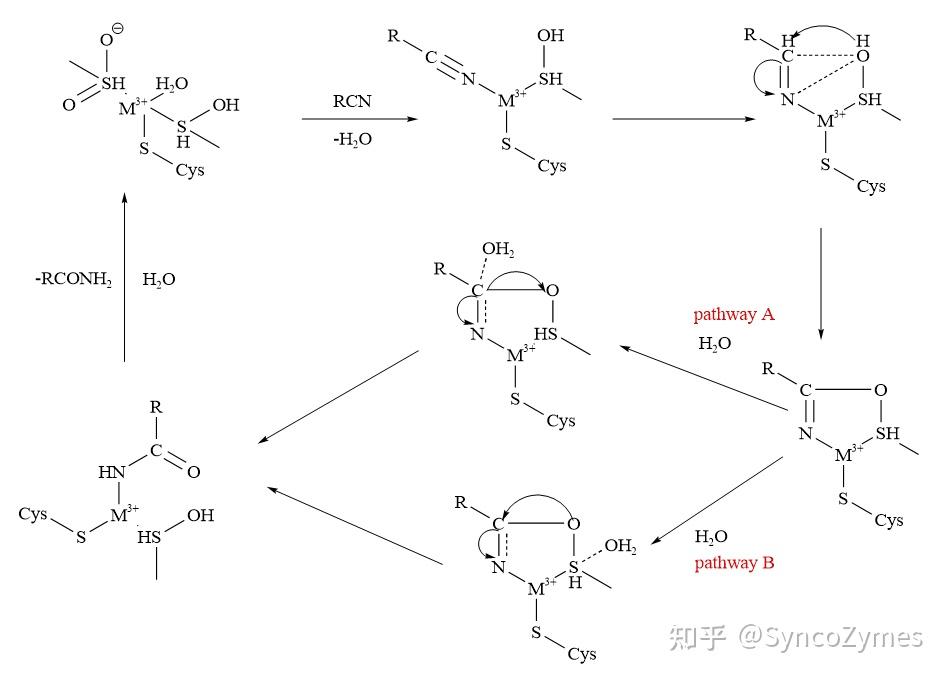
三、304am永利集团生物腈水合酶酶庫和酶開發服務介紹
304am永利集团生物從(cong) 2007年來就專(zhuan) 注於(yu) 生物酶和生物催化技術以及合成生物學技術的開發與(yu) 應用研究。304am永利集团生物現有的腈水合酶酶庫(304am永利集团生物代號:ES-NHT)中包含24種不同的腈水合酶,可以為(wei) 客戶提供酶篩選、酶促反應工藝優(you) 化、酶改造和生產(chan) 供應服務。
四、參考文獻
[1] Nagashima S, Nakasako M, Dohmae N, et al. Nature Structural Biology, 1998, 5(5): 347.
[2] Miyanaga A, Fushinobu S, Ito K, et al.European Journal of Biochemistry, 2004, 271(2): 429-438.
[3] Arakawa T, Kawano Y, Kataoka S, et al.Journal of Molecular Biology, 2007, 366(5): 1497-1509.
[4] Brodkin H R, Novak W R, Milne A C, et al.Biochemistry, 2011, 50(22): 4923-4935.
[5] Song L, Wang M, Shi J, et al.Biochemical and Biophysical Research Communications, 2007, 362(2): 319-324.
[6] 郭軍(jun) 玲, 高性能腈水合酶的挖掘及半理性改造. [D] 無錫: 江南大學, 2023.
[7] Vojtech V., Ludmila M., Alicja B. V., e tal. J Mol Catal B-enzym, 2011,71: 51-55.
[8] 曾文彬, 異羥肟酸類衍生物的設計、合成、結構分析及抗腫瘤活性研究. [D] 江西:南昌大學, 2013.
[9] 馬東(dong) , 基於(yu) 半理性設計改造腈水合酶的底物譜和催化性能. [D] 無錫: 江南大學, 2024.
搜索


-
-

